400-998-5282
专注多肽 服务科研
400-998-5282
专注多肽 服务科研
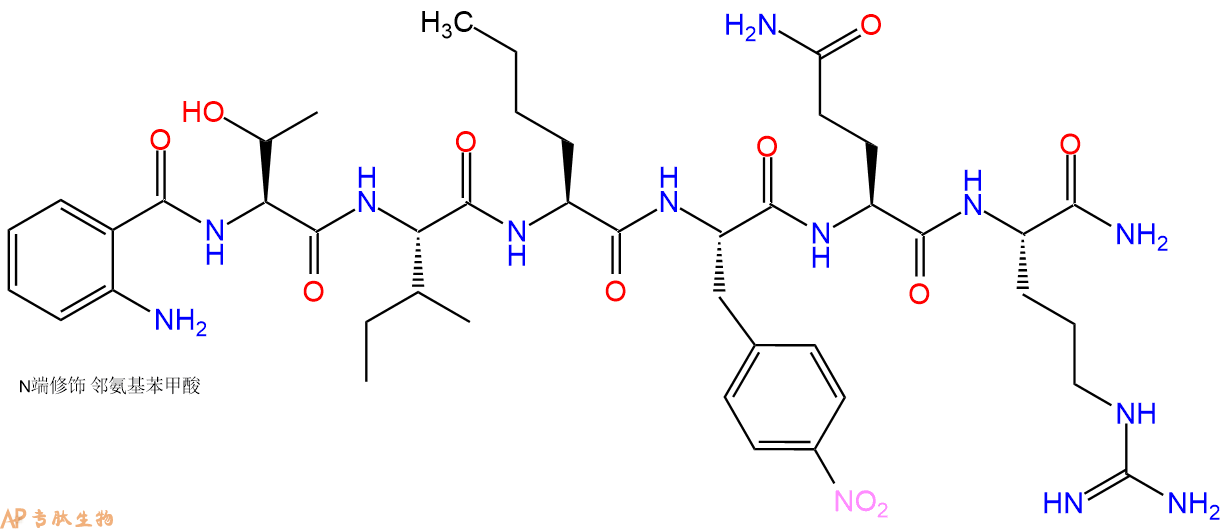
这种六肽 FRET 底物来源于病毒 gag-pol 多蛋白的 p24/p15 切割位点。已经开发出一种简单、连续的 HIV 蛋白酶荧光测定法,可以筛选潜在的 HIV 蛋白酶抑制剂。Km (2.1 μM) 和 kcat (7.4 s⁻¹) 的值由低酶浓度下的稳态数据计算得出。激发波长为 280 nm,发射波长 > 435 nm。
编号:200060
CAS号:133233-38-2
单字母:Abz-TI-Nle-F(4NO2)-QR-CONH2
| 编号: | 200060 |
| 中文名称: | 蒽基HIV蛋白酶底物、Anthranilyl-HIV Protease Substrate |
| 英文名: | Anthranilyl-HIV Protease Substrate |
| CAS号: | 133233-38-2 |
| 单字母: | Abz-TI-Nle-F(4NO2)-QR-CONH2 |
| 三字母: | Abz N端Abz修饰,2-氨基苯甲酰基或邻氨基苯甲酰基(Abz),是一种荧光染料,其激发波长为320纳米,发射波长为420纳米。 -ThrL-苏氨酸:threonine。系统命名为(2S)-氨基-(3R)-羟基丁酸。有两个手性中心,是编码氨基酸。是哺乳动物的必需氨基酸。符号:T,Thr。 -IleL-异亮氨酸:isoleucine。系统命名为(2S)-氨基-(3R)-甲基戊酸。是编码氨基酸。有两个手性碳原子,是哺乳动物的必需氨基酸。符号:I,Ile。 -Nle正亮氨酸 -Phe(4NO2)对硝基苯丙氨酸、para-nitro-phenylalanine -GlnL-谷氨酰胺:glutamine。系统命名为(2S)-氨基-4-氨酰基丁酸,是编码氨基酸。符号:GIn,Q。 -ArgL-精氨酸:arginine。系统命名为(2S)-氨基-5-胍基戊酸。在生理条件下带正电荷,为编码氨基酸。是幼小哺乳动物的必需氨基酸。符号:R,Arg。 -CONH2C端酰胺化 |
| 氨基酸个数: | 6 |
| 分子式: | C43H65N13O11 |
| 平均分子量: | 940.06 |
| 精确分子量: | 939.49 |
| 等电点(PI): | - |
| pH=7.0时的净电荷数: | 1 |
| 平均亲水性: | -0.55 |
| 疏水性值: | 0.4 |
| 消光系数: | - |
| 来源: | 人工化学合成,仅限科学研究使用,不得用于人体。 |
| 储存条件: | 负80℃至负20℃ |
| 标签: | 人类免疫缺陷病(HIV)肽 氨基酸衍生物肽 酶底物肽(Substrate Peptide) 侧链保护基肽 Abz标记肽 |
This hexapeptide FRET substrate is derived from the p24/p15 cleavage site of the viral gag-pol poly-protein. A simple, continuous fluorometric assay for HIV protease has been developed, which allows the screening of potential HIV protease inhibitors. Values for Km (2.1 μM) and kcat (7.4 s⁻¹) were calculated from steady-state data at a low concentration of the enzyme. Excitation at 280 nm, emission at > 435 nm.
邻氨基苯甲酰基 - HIV 蛋白酶底物三氟乙酸盐:采用邻氨基苯甲酰基荧光团,高灵敏度监测切割行为,肽序列支持催化周转动力学表征,三氟乙酸盐形式确保分析流程中溶解度一致性,可用于抑制剂筛选、机制酶学与蛋白酶特异性谱分析。
Anthranilyl-HIV Protease Substrate employs an anthranilyl fluorophore to monitor cleavage behavior with high sensitivity. The peptide sequence supports kinetic characterization of catalytic turnover. Its trifluoroacetate form ensures consistent solubility for analytical workflows. Researchers use it in inhibitor screening, mechanistic enzymology, and protease-specific profiling.
Definition
Human immunodeficiency virus (HIV) is a lentivirus that causes acquired immunodeficiency syndrome (AIDS), a condition in humans in which the immune system begins to fail, leading to life-threatening opportunistic infections. Over 5000 HIV-related peptides have been synthesized, that inhibit different stages of viral life cycle.
Discovery
In 1983, two separate researchers Robert Gallo and Luc Montagnier independently declared that a novel retrovirus infecting AIDS patients. Several HIV related peptides including peptides (15-mers or 20-mers) of HIV glycoprotein 160 (gp160), gp120W16D, MN envelope (env) consensus B tat, consensus B VIF, HXB2 gag, SIVmac239, SIVmac239env, SIVmac239 gag have been used to study HIV life cycle. C34 peptide of Gp41 HIV Fragment is known as HR2, belongs to the helical region of gp41 of HIV, C-terminal heptad repeat 2 (HR2) defined as C helix or C peptide. It is known that HIV-1 enters cells by membrane fusion, C34 gp41 peptide is a potent inhibitors of HIV-1 fusion 1,2. The 86 amino acid trans-activator (Tat) protein of human immunodeficiency virus type 1 (HIV-1) is an RNA-binding transcriptional regulator. HIV-1 Tat proteins (wild type and Thr40Lys mutant) and the HIV-1 Tat peptide fragments Tat(32–48) and Tat(32–72) were chemically synthesized and used for HIV studies 3.
HIV (gp120) fragment (254-274), this fragment with sequence homology to a domain of the external envelope glycoprotein (gp120) of the human immunodeficiency virus (HIV) is important for HIV infectivity and antibody neutralization 4. HIV (gp120) fragment (421-438), derived from the CD4 attachment region of HIV gp120, inhibited the syncytial formation in vitro 5. HIV-1 gag protein p17 (76-84), HLA-A*0201-restricted immunodominant CD8 epitope of the HIV gag protein used for the characterization of CD8+ -T cells of HIV-positiv patients 6. HIV-1 rev protein (34-50), this arginine-rich fragment interacts specifically with RNA. It has been shown that rev protein and rev protein (34-50) bind IIB RNA with a similar dissociation constant of approx. 10 nM 7.
Structural Characteristics
The HIV type-1 belongs to the family Retroviridae and consists of two basic components: a core of ribonucleic acid (RNA), called the genome, and a protein component that surrounds the genome, called a capsid. The single-stranded RNA is tightly bound to nucleocapsid proteins and enzymes needed for the morphogenesis of the virion such as reverse transcriptase, proteases, ribonuclease and integrase. A matrix composed of the viral protein that surrounds the capsid. Viral envelope is composed of two layers of fatty molecules taken from the membrane of a human cell during budding process. There are 70 copies of a complex HIV protein that protrudes through the surface of the virus particle, known as Env, consists of a cap, glycoprotein (gp) 120, and a stem, gp41 molecules. This glycoprotein complex is important for fusion of virus to host cell. Both these surface proteins are important targets for treatments or HIV vaccines 8.
Mode of Action
HIV binds to a CD4 receptor and one of two co-receptors on the surface of a CD4+ T- lymphocyte. After fusion, the virus releases RNA, its genetic material, into the host cell. An HIV enzyme called reverse transcriptase converts the single- stranded HIV RNA to double-stranded HIV DNA. The newly formed HIV DNA enters the host cell's nucleus. The integrated HIV DNA is called provirus. The provirus may remain inactive for several years, producing few or no new copies of HIV. When the host cell receives a signal to become active, the provirus uses a host enzyme called RNA polymerase to create copies of the HIV genomic material, as well as shorter strands of RNA called messenger RNA (mRNA). The mRNA is used as a blueprint to make long chains of HIV proteins. An HIV enzyme called protease cuts the long chains of HIV proteins into smaller individual proteins. As the smaller HIV proteins come together with copies of HIV's RNA genetic material, a new virus particle is assembled. The newly assembled virus buds out from the host cell. During budding, the new virus acquires part of the cell's outer envelope. This envelope is embedded with viral glycoproteins which are necessary for host cell recognition.
Functions
CD8 cytotoxic, HIV-1 specific CD8 cytotoxic T lymphocyte (CTL) responses play a critical role in controlling HIV-1 replication. TCR avidity correlates with CTL function, and CTLs expressing TCRs with high avidity for their cognate MHC-viral peptide complex play an important in vivo role in neutralizing virus infections, terminating virus infection and delaying systemic AIDS virus dissemination from the mucosal inoculation site.
HIV-1 envelope transmembrane protein that contain highly positively charged amphipathic helices (designated LLP) in have both cytolytic and calmodulin (CaM) binding/inhibitory properties that contribute to cytopathogenesis during a viral infection.
HIV-1 vif, The human immunodeficiency virus type 1 (HIV-1) auxiliary gene vif is essential for virus propagation in peripheral blood lymphocytes, macrophages, and in some T-cell lines. (i) Vif protein binds HIV-1 PR (protease), but not covalently linked tethered PR-PR; (ii) the four amino acids residing at the N terminus of HIV-1 PR are essential for Vif/PR interaction; (iii) synthetic peptide derived from the N terminus of HIV-1 PR inhibits Vif/PR binding; and (iv) this peptide inhibits the propagation of HIV-1 in restrictive cells 9.
References
1. Bianchi E, Finotto M, Ingallinella P, Hrin R, Carella AV, Hou XS, Schleif WA, Miller MD, Geleziunas R, Pessi A (2005). Covalent stabilization of coiled coils of the HIV gp41 N region yields extremely potent and broad inhibitors of viral infection. PNAS., 102(36):12903-12908
2. de Rosny E, Vassell R, Jiang S, Kunert R, Weiss CD (2004). Binding of the 2F5 monoclonal antibody to native and fusion-intermediate forms of human immunodeficiency virus type 1 gp41: implications for fusion-inducing conformational changes. J. Virol., 78(5):2627-2631.
3. Klostermeier D, Bayer P, Kraft M, Frank RW, Rösch P (1997). Spectroscopic investigations of HIV-1 trans-activator and related peptides in aqueous solutions. Biophysical Chemistry, 63(2):87-96.
4. Ho DD, Kaplan JC, Rackauskas IE, Gurney ME (1988). Second conserved domain of gp120 is important for HIV infectivity and antibody neutralization. Science, 239(4843):1021-1023.
5. Morrow WJ, Williams WM, Whalley AS, Ryskamp T, Newman R, Kang CY, Chamat S, Köhler H, Kieber-Emmons T (1992). Synthetic peptides from a conserved region of gp120 induce broadly reactive anti-HIV responses. Immunology, 75(4):557-564.
6. Wilkinson J, Cope A, Gill J, Bourboulia D, Hayes P, Imami N, Kubo T, Marcelin A, Calvez V, Weiss R, Gazzard B, Boshoff C, Gotch F (2002). Identification of Kaposi's sarcoma-associated herpesvirus (KSHV)-specific cytotoxic T-lymphocyte epitopes and evaluation of reconstitution of KSHV-specific responses in human immunodeficiency virus type 1-Infected patients receiving highly active antiretroviral therapy. J. Virol., 76(6):2634-2640.
7. Kjems J, Calnan BJ, Frankel AD, Sharp PA (1992). Specific binding of a basic peptide from HIV-1 Rev. EMBO J., 11(3):1119-29.
8. Chan DC, Fass D, Berger JM, Kim PS (1997). Core structure of gp41 from the HIV envlope glycoprotein . Cell, 89:263–73.
9. Hutoran M, Britan E, Baraz L, Blumenzweig I, Steinitz M, Kotler M (2004). Abrogation of Vif function by peptide derived from the N-terminal region of the human immunodeficiency virus type 1 (HIV-1) protease. Virology, 330(1):261-270.
Caspase酶对应的底物,Caspases(半胱氨酸天冬氨酸蛋白酶,半胱氨酸依赖性天冬氨酸定向蛋白酶)是一类蛋白酶家族,其功能与凋亡(程序性细胞死亡),坏死和发烧(炎症)的过程密切相关。

什么是胱天蛋白酶?
胱天蛋白酶(Caspases)是含半胱氨酸的天冬氨酸蛋白水解酶,它们是为细胞凋亡的主要介质。多种受体,例如TNF-α 受体,FasL受体,TLR和死亡受体,以及Bcl-2和凋亡抑制剂(IAP)蛋白家族参与并调节该caspase依赖性凋亡途径。一旦Caspase受到上游信号(外部或内在)刺激被激活,即会参与执行下游蛋白底物的水解作用,并触发一系列事件,导致细胞分解,死亡,吞噬作用和细胞碎片的清除。
人Caspases酶
人的Caspases家族基于序列相似性和生物学功能等共性主要可分为三大类:第一类由具有长胱天蛋白酶募集结构域的“炎症”胱天蛋白酶组成,他们对P4位上的较大的芳香族或疏水性残基具有亲和力。第二类由具有短的前体结构域的“细胞凋亡效应”胱天蛋白酶组成,而第三类由具有长的前提结构域的Pap位置具有亮氨酸或缬氨酸底物亲和力的“凋亡引发剂”胱天蛋白酶组成(表1)。
表1. 人胱天蛋白酶的功能分类:
| 细胞死亡途径 | 半胱天冬酶类型 | 酵素 | 物种 |
| 细胞凋亡 | 启动器 | Caspases 2 | 人与鼠 |
| 细胞凋亡 | 启动器 | Caspases 8 | 人与鼠 |
| 细胞凋亡 | 启动器 | Caspases 9 | 人与鼠 |
| 细胞凋亡 | 启动器 | Caspases 10 | 人的 |
| 细胞凋亡 | 效应器 | Caspases 3 | 人与鼠 |
| 细胞凋亡 | 效应器 | Caspases 6 | 人与鼠 |
| 细胞凋亡 | 效应器 | Caspases 6 | 人与鼠 |
| 细胞焦亡 | 炎性的 | Caspases 1 | 人与鼠 |
| 细胞焦亡 | 炎性的 | Caspases 4 | 人的 |
| 细胞焦亡 | 炎性的 | Caspases 5 | 人的 |
启动器Caspase和效应器Caspase酶
根据其在凋亡胱天蛋白酶途径中的作用,胱天蛋白酶可分为两类:启动器和效应器Caspase酶。启动器和效应器Caspas酶都具有由小亚基和大亚基组成的催化位点,Caspase酶的识别位

凋亡启动器Caspase酶,例如caspase-2,-8,-9和-10可以启动caspase激活级联反应。Caspase-8对于形成死亡诱导信号复合物(DISC)是必不可少的,并且在激活后,Caspase-8激活下游效应子Caspase(例如Caspase 3)并介导线粒体中细胞色素c的释放。Caspase-8已被证明对IETD肽序列具有相对较高的底物选择性。凋亡效应胱天蛋白酶例如Caspase-3,-6和-7虽然不负责启动级联途径,但是当被激活时,它们在级联的中间和后续步骤中起着不可或缺的作用。Caspase-3(CPP32 / apopain)是关键效应器,因为它放大了来自启动器Caspase的信号,使用对Caspase-3有选择性的DEVD肽序列对活化的Caspase-3进行检测,可以检测Caspase-3的活性。
Caspase酶底物和抑制剂
Caspase底物和抑制剂由两个关键成分组成:Caspase识别序列和信号产生或蛋白酶抑制基序。不同Caspase识别序列不同,一般由三个或四个氨基酸组成(表2)。Caspase酶识别序列的N端通常有乙酰基(Ac)或碳苯甲氧基(Z)基团修饰,以增强膜的通透性。对应的Caspase识别特定的肽序列为其酶促反应切割位点,释放产生信号或抑制信号的基序。Caspase的显色和荧光底物均以相似的方式起作用,其中底物的信号或颜色强度与蛋白水解活性成正比。
表2. Caspase的底物及其序列
| 多肽 | 氨基酸序列 | 对应的Caspase的种类 |
| IETD | Ile-Glu-Thr-Asp | Caspase 8,颗粒酶B |
| DEVD | Asp-Glu-Val-Asp | Caspase 3、6、7、8或10 |
| LEHD | Leu-Glu-His-Asp | Caspase 9 |
| VAD | Val-Ala-Asp | Caspase 1、2、3、6、8、9或10 |
Caspase酶的显色底物
Caspase的显色底物是有Caspase识别序列及生色基团组成,常见的生色团有pNA(对硝基苯胺或4-硝基苯胺),可使用酶标仪或分光光度计在405 nm处进行光密度检测。
表3. Caspase的显色底物
| 底物 | Caspase | 吸收(nm) | 颜色 |
| Ac-DEVD-pNA * CAS 189950-66-1 * | 半胱天冬酶3 | 405 nm | 黄色 |
| Z-DEVD-pNA | 半胱天冬酶3 | 405 nm | 黄色 |
| Z-IETD-pNA * CAS 219138-21-3 * | 半胱天冬酶8,颗粒酶B | 405 nm | 黄色 |
Caspase的荧光底物
Caspase的荧光底物的结构包含与半胱天冬酶识别相关的荧光团,例如7-氨基-4-甲基香豆素(AMC),7-氨基-4-三氟甲基香豆素(AFC), Rhodamine 110(R110)或ProRed™620。R110的Caspase底物比基于香豆素的Caspase底物(例如AMC和AFC)更敏感,但由于两步裂解过程,其动态范围更窄。 建议将R110标记的Caspase底物用于终点法测定,而将AMC和AFC标记的 Caspase底物用于动力学测定。

图.从左到右,分别是AMC(7-氨基-4-甲基香豆素),AFC(7-氨基-4-三氟甲基香豆素),Rhodamine 110(R110)和ProRed™620的激发和发射光谱。
表4.荧光半胱天冬酶底物。
| 底物名称 | 对应的Caspase | Ex(nm) | Em(nm) | ε¹ | Φ² |
| Ac-DEVD-AFC * CAS 201608-14-2 * | 半胱天冬酶3、7 | 376 | 482 | 17000 | 0.53 |
| Ac-DEVD-AMC * CAS 169332-61-0 * | 半胱天冬酶3、7 | 341 | 441 | 19000 | N / D |
| Z-DEVD-AFC | 半胱天冬酶3、7 | 376 | 482 | 17000 | 0.53 |
| Z-DEVD-AMC * CAS 1135416-11-3 * | 半胱天冬酶3、7 | 341 | 441 | 19000 | N / D |
| Z-DEVD-ProRed™620 | 半胱天冬酶3、7 | 532 | 619 | N / D | N / D |
| (Z-DEVD)2 -R110 * CAS 223538-61-2 * | 半胱天冬酶3、7 | 500 | 522 | 80000 | N / D |
| Z-DEVD-ProRed™620 | 半胱天冬酶3、7 | 532 | 619 | N / D | N / D |
| Ac-IETD-AFC * CAS 211990-57-7 * | 半胱天冬酶8,颗粒酶B | 376 | 482 | 17000 | 0.53 |
| Z-IETD-AFC * CAS 219138-02-0 * | 半胱天冬酶8,颗粒酶B | 376 | 482 | 17000 | 0.53 |
注意:
1.ε=在其最大吸收波长处的摩尔消光系数(单位= cm -1M -1)。
2.Φ=水性缓冲液(pH 7.2)中的荧光量子产率。
Caspase抑制剂
Caspase抑制剂能与Caspase的活性位点结合并形成可逆或不可逆的连接,通常,Caspase抑制剂的结构由Caspase识别序列,诸如醛(-CHO)或氟甲基酮(-FMK)的官能团组成。具有醛官能团的胱天蛋白酶抑制剂是可逆的,而具有FMK的抑制剂是不可逆的。半胱天冬酶底物和抑制剂都具有较小的细胞毒性作用,因此,它们是研究半胱天冬酶活性的有用工具。
表5. 可逆和不可逆的Caspase酶抑制剂
| 抑制剂 | Caspase的种类 | 是否可逆 | Ex(nm) | Em(nm) |
| Ac-DEVD-CHO * CAS 169332-60-9 * | 半胱天冬酶3、7 | 可逆的 | -- | -- |
| Ac-IETD-CHO * CAS 191338-86-0 * | 半胱天冬酶8 | 可逆的 | -- | -- |
| mFluor™450-VAD-FMK | 半胱天冬酶1,2,3,6,8,9,10 | 不可逆的 | 406 | 445 |
| mFluor™510-VAD-FMK | 半胱天冬酶1,2,3,6,8,9,10 | 不可逆的 | 412 | 505 |
| FITC-C6-DEVD-FMK | 半胱天冬酶3、7 | 不可逆的 | 491 | 516 |
| FITC-C6-DEVD-FMK | 半胱天冬酶3、7 | 不可逆的 | 491 | 516 |
| FITC-C6-LEHD-FMK | 半胱天冬酶9 | 不可逆的 | 491 | 516 |
| FITC-C6-LEHD-FMK | 半胱天冬酶9 | 不可逆的 | 491 | 516 |
| FAM-VAD-FMK | 半胱天冬酶1,2,3,6,8,9,10 | 不可逆的 | 493 | 517 |
| SRB-VAD-FMK [磺胺丁胺B-VAD-FMK] | 半胱天冬酶1,2,3,6,8,9,10 | 不可逆的 | 559 | 577 |
Abz标记肽的说明:
2-Aminobenzoyl, or Anthraniloyl, (Abz) is a fluorophor with an excitation at 320 nm ▉ and emission of 420 nm ▉.
| DOI | 名称 | |
|---|---|---|
| 10.1021/bi0116543 | HIV-1 protease: characterization of a catalytically competent enzyme-substrate intermediate | 下载 |
| 10.1021/bi011781z | Anisotropic dynamics of the JE-2147-HIV protease complex: drug resistance and thermodynamic binding mode examined in a 1.09 A structure | 下载 |
| 10.1002/cmdc.200500063 | A potent HIV protease inhibitor identified in an epimeric mixture by high-resolution protein crystallography | 下载 |
| 10.1021/jm701142s | Structure-guided design of C2-symmetric HIV-1 protease inhibitors based on a pyrrolidine scaffold | 下载 |
| 10.1021/jm800149m | A copper(I)-catalyzed 1,2,3-triazole azide-alkyne click compound is a potent inhibitor of a multidrug-resistant HIV-1 protease variant | 下载 |
| 10.1002/cmdc.200900452 | Pyrrolidine derivatives as plasmepsin inhibitors: binding mode analysis assisted by molecular dynamics simulations of a highly flexible protein | 下载 |
| 10.1111/j.1399-3011.1990.tb00994.x | A simple, continuous fluorometric assay for HIV protease | 下载 |
| 10.1016/j.jmb.2011.04.052 | Two solutions for the same problem: multiple binding modes of pyrrolidine-based HIV-1 protease inhibitors | 下载 |
| 10.1016/j.jmb.2011.03.038 | Accessory mutations maintain stability in drug-resistant HIV-1 protease | 下载 |
| 10.1021/jm300072d | Potent antiviral HIV-1 protease inhibitor GRL-02031 adapts to the structures of drug resistant mutants with its P1'-pyrrolidinone ring | 下载 |
| 10.1021/jm301519z | Novel P2 tris-tetrahydrofuran group in antiviral compound 1 (GRL-0519) fills the S2 binding pocket of selected mutants of HIV-1 protease | 下载 |
| 10.1002/anie.201309682 | Structure-based design of inhibitors of the aspartic protease endothiapepsin by exploiting dynamic combinatorial chemistry | 下载 |
| 10.1021/cb5009487 | Colloidal aggregation and the in vitro activity of traditional Chinese medicines | 下载 |
| 10.1021/acs.jmedchem.5b00474 | Substituted Bis-THF Protease Inhibitors with Improved Potency against Highly Resistant Mature HIV-1 Protease PR20 | 下载 |
| 10.1073/pnas.90.24.11638 | Catalytic contribution of flap-substrate hydrogen bonds in "HIV-1 protease" explored by chemical synthesis | 下载 |
| 10.1128/jvi.76.3.1359-1368.2002 | Altered substrate specificity of drug-resistant human immunodeficiency virus type 1 protease | 下载 |
| 10.1016/j.jmb.2008.07.062 | Structural and kinetic analysis of pyrrolidine-based inhibitors of the drug-resistant Ile84Val mutant of HIV-1 protease | 下载 |
| 10.1021/bi200033z | The L76V drug resistance mutation decreases the dimer stability and rate of autoprocessing of HIV-1 protease by reducing internal hydrophobic contacts | 下载 |
| 10.1021/jm3001136 | Synthesis and biological activity of potent HIV-1 protease inhibitors based on Phe-Pro dihydroxyethylene isosteres | 下载 |
多肽Abz-Thr-Ile-Nle-Phe(4NO2)-Gln-Arg-NH2的合成步骤:
1、合成MBHA树脂:取若干克MBHA树脂(如初始取代度为0.5mmol/g)和1倍树脂摩尔量的Fmoc-Linker-OH加入到反应器中,加入DMF,搅拌使氨基酸完全溶解。再加入树脂2倍量的DIEPA,搅拌混合均匀。再加入树脂0.95倍量的HBTU,搅拌混合均匀。反应3-4小时后,用DMF洗涤3次。用2倍树脂体积的10%乙酸酐/DMF 进行封端30分钟。然后再用DMF洗涤3次,甲醇洗涤2次,DCM洗涤2次,再用甲醇洗涤2次。真空干燥12小时以上,得到干燥的树脂{Fmoc-Linker-MHBA Resin},测定取代度。这里测得取代度为 0.3mmol/g。结构如下图:

2、脱Fmoc:取2.84g的上述树脂,用DCM或DMF溶胀20分钟。用DMF洗涤2遍。加3倍树脂体积的20%Pip/DMF溶液,鼓氮气30分钟,然后2倍树脂体积的DMF 洗涤5次。得到 H2N-Linker-MBHA Resin 。(此步骤脱除Fmoc基团,茚三酮检测为蓝色,Pip为哌啶)。结构图如下:

3、缩合:取2.56mmol Fmoc-Arg(Pbf)-OH 氨基酸,加入到上述树脂里,加适当DMF溶解氨基酸,再依次加入5.11mmol DIPEA,2.43mmol HBTU。反应30分钟后,取小样洗涤,茚三酮检测为无色。用2倍树脂体积的DMF 洗涤3次树脂。(洗涤树脂,去掉残留溶剂,为下一步反应做准备)。得到Fmoc-Arg(Pbf)-Linker-MBHA Resin。氨基酸:DIPEA:HBTU:树脂=3:6:2.85:1(摩尔比)。结构图如下:

4、依次循环步骤二、步骤三,依次得到
H2N-Arg(Pbf)-Linker-MBHA Resin
Fmoc-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
H2N-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
Fmoc-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
H2N-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
Fmoc-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
H2N-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
Fmoc-Ile-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
H2N-Ile-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
Fmoc-Thr(tBu)-Ile-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin
以上中间结构,均可在专肽生物多肽计算器-多肽结构计算器中,一键画出。
最后再经过步骤二得到 H2N-Thr(tBu)-Ile-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHA Resin,结构如下:

5、邻氨基苯甲酸反应连接:在上述树脂中,加入适当DMF后,再加入2.56mmol 邻氨基苯甲酸到树脂中,再加入5.11mmol DIPEA、2.43mmol HBTU,鼓氮气反应30分钟。用2倍树脂体积的DMF 洗涤3次树脂(洗涤树脂,去掉残留溶剂,为下一步反应做准备)。 得到Abz-Thr(tBu)-Ile-Nle-Phe(4NO2)-Gln(Trt)-Arg(Pbf)-Linker-MBHAResin。 结构如下:
5、切割:6倍树脂体积的切割液(或每1g树脂加8ml左右的切割液),摇床摇晃 2小时,过滤掉树脂,用冰无水乙醚沉淀滤液,并用冰无水乙醚洗涤沉淀物3次,最后将沉淀物放真空干燥釜中,常温干燥24小试,得到粗品Abz-Thr-Ile-Nle-Phe(4NO2)-Gln-Arg-NH2。结构图见产品结构图。
切割液选择:1)TFA:H2O=95%:5%、TFA:H2O=97.5%:2.5%
2)TFA:H2O:TIS=95%:2.5%:2.5%
3)三氟乙酸:茴香硫醚:1,2-乙二硫醇:苯酚:水=87.5%:5%:2.5%:2.5%:2.5%
(前两种适合没有容易氧化的氨基酸,例如Trp、Cys、Met。第三种适合几乎所有的序列。)
6、纯化冻干:使用液相色谱纯化,收集目标峰液体,进行冻干,获得蓬松的粉末状固体多肽。不过这时要取小样复测下纯度 是否目标纯度。
7、最后总结:
杭州专肽生物技术有限公司(ALLPEPTIDE https://www.allpeptide.com)主营定制多肽合成业务,提供各类长肽,短肽,环肽,提供各类修饰肽,如:荧光标记修饰(CY3、CY5、CY5.5、CY7、FAM、FITC、Rhodamine B、TAMRA等),功能基团修饰肽(叠氮、炔基、DBCO、DOTA、NOTA等),同位素标记肽(N15、C13),订书肽(Stapled Peptide),脂肪酸修饰肽(Pal、Myr、Ste),磷酸化修饰肽(P-Ser、P-Thr、P-Tyr),环肽(酰胺键环肽、一对或者多对二硫键环),生物素标记肽,PEG修饰肽,甲基化修饰肽
以上所有内容,为专肽生物原创内容,请勿发布到其他网站上。





